Serviços Personalizados
Artigo
Indicadores
 Citado por SciELO
Citado por SciELO
Links relacionados
 Similares em
SciELO
Similares em
SciELO
Bookmark
Revista USP
versão impressa ISSN 0103-9989
Rev. USP no.89 São Paulo mar./maio 2011
Organismos transgênicos no Brasil: regular ou desregular?
Walter Colli
Professor titular aposentado do Departamento de Bioquímica, do Instituto de Química da USP
RESUMO
A análise de risco de OGM ou transgênicos segue protocolos internacionais através das quais se pergunta sobre o possível dano (efeito adverso), a forma de aparecimento do dano (riscos), os riscos significativos que mereçam análise detalhada e de que forma o risco identificado será observado e medido (avaliação). Assim como no Brasil, análises de risco efetuadas em outros países nos últimos quinze anos nunca evidenciaram, nos produtos liberados, efeitos adversos à saúde humana e animal ou ao ambiente. O excesso de regulamentação favorece as grandes empresas que têm recursos e tempo para atender a todas as demandas regulatórias. No entanto, pequenas empresas ou estatais como a Embrapa não têm orçamento para cumprir com os exageros do excesso de regulamentação. Por isso, o Brasil, tendo em vista a experiência dos outros países, além de sua própria experiência, deve introduzir mais racionalidade no debate e começar a desregular o que está regulado em demasia.
As plantas transgênicas, além de inócuas, trazem vantagens econômicas e ao meio ambiente. Comprovadamente, reduzem o uso de água por exigir menos inseticidas e economizam o uso de óleo diesel reduzindo a emissão de CO2 na atmosfera.
Palavras-chave: transgênicos, análises de risco, saúde, ambiente.
ABSTRACT
The risk analysis of GMOs or transgenic plants follows international protocols concer-ning with possible damages (adverse effects), the form in which damages occur (risks), the significant risks deserving a thorough analysis, and which way the identified risk is to be observed and measured (assessment). Just like what has happened in Brazil, risk analyses conducted in other countries in the last fifteen years have never found any market-released products with adverse effects to human or animal health or to the environment. The excessive regulation favors big companies, which have resources and time to meet all regulatory demands. On the other hand, small-sized companies or state companies such as Embrapa do not have enough budgeting to comply with the overburdening regulation. Thus, taking into account the experience of other countries and also its own experience, Brazil should address this debate with more rationality, and start de-regulating what is over-regulated.
Transgenic plants are harmless, and also favorable to the economy and to the environment. It has been proved that they reduce water use as they demand less insecticide, and also the use of diesel oil, thus reducing CO2 emission into the atmosphere.
Keywords: transgenic plants, risk analyses, health, environment.
"Civilization has been built on genetically modified plants" (Nina V. Fedoroff).
INTRODUÇÃO
Em 10 de agosto de 1999, Antônio Souza Prudente, juiz federal da 60ª Vara, Seção Judiciária do Distrito Federal, exarou sentença (processos nº N1 1998.34.00.027681-8, classe 9200, de 10/8/1999, e 1998.34.00.027682-0, Classe 7100, de 26/6/2000) em ação cautelar ajuizada pelo Idec, tendo como litisconsortes o Greenpeace e o Ibama, visando impedir, imediatamente, a autorização para qualquer pedido de plantio da soja transgênica (round up ready), antes que se procedesse à devida regulamentação da matéria e ao prévio Estudo e Relatório de Impacto Ambiental (EIA/Rima).
À época, em 1998, a Comissão Técnica Nacional de Biotecnologia (CTNBio), constituída conforme a Lei 8.974/95, havia aprovado a liberação comercial desse produto por não encontrar evidência de danos ao ambiente e à saúde.
Dentre as diversas considerações do juiz Prudente que fundamentaram suas conclusões e levaram à suspensão da decisão da CTNBio encontra-se a seguinte pérola in verbis:
"Sem contabilizar exageros, creio que a velocidade irresponsável que se pretende imprimir nos avanços da engenharia genética, nos dias atuais, guiada pela desregulamentação gananciosa da globalização econômica, poderá gestar, nos albores do novo milênio, uma esquisita civilização de 'aliens hospedeiros' com fisionomia peçonhenta, a comprometer, definitivamente, em termos reais, e não fictícios, a sobrevivência das futuras gerações do nosso planeta".
Outras considerações desse jaez arrematadas com as expressões latinas fumus boni iuris e periculum in mora, vazias de conteúdo como um balão furado, mas sempre muito usadas por alguns procuradores e juízes para contestar evidências científicas sólidas, levaram a uma sentença que paralisou a biotecnologia brasileira por cinco anos com todas as consequências ulteriores. Quando se fala em paralisação não se está referindo apenas aos prejuízos do detentor da patente, mas ao desestímulo global à ciência e à tecnologia no Brasil.
Faltou ao juiz conhecimento de biologia. É preciso urgentemente que o Poder Judiciário agregue competência técnica antes de tomar decisões evitando, assim, sentenças calcadas no desconhecimento e na ideologia. Um gene nada mais é do que um pedaço de informação que pode ser sintetizada quimicamente em laboratório e usada em diferentes organismos, como uma palavra pode ser usada em vários contextos. Todos os organismos vivos estão relacionados uns aos outros e compartilham o mesmo sistema genético de tal modo que um gene de um organismo pode funcionar muito bem em outro. Pode-se colocar um gene de macaco numa fruta ou de uma fruta no macaco. Os genes do macaco ou da fruta são peças de informação e não carregam uma marca dizendo: "eu vim do macaco ou da fruta".
Essa sentença somente foi revertida em sede de recurso de apelação junto ao TRF da 1ª região, onde restou vencedor em 28/6/2004 o magnífico voto da relatora, desembargadora federal Selene Maria de Almeida, em Apelação Cível nº 1998.34.00.027682-0/DF (710 páginas, 3 volumes, 2004), que discutiu, dentre outros aspectos, a aplicação do princípio da precaução, argumento dos reclamantes abrigado pelo juiz Prudente.
Coisa parecida aconteceu nos EUA, mas 24 anos antes. Em 1975, os cientistas que desenvolveram os primeiros experimentos com DNA recombinante convocaram uma reunião em Asilomar, na Califórnia. Talvez um pouco inflados com a própria importância e com o aparente poder que lhes conferia o fato de saberem manipular o DNA, criaram regras para essa manipulação e agitaram a mídia. Isso aumentou a percepção popular sobre possíveis riscos no trabalho com DNA recombinante. Esse receio foi capitalizado pelo prefeito de Cambridge, cujo nome era Vellucci. Esse homem, em 1977 escreveu para o presidente da Academia Nacional de Ciências (apud Watson, 2005):
"Na edição de hoje do Boston Herald American, uma publicação do grupo Hearst, há duas reportagens que muito me preocuparam. Em Dover, Massachusetts, 'uma estranha criatura de olhos alaranjados' foi avistada. Em Hollis, New Hampshire, um homem e seus dois filhos se depararam com 'uma criatura peluda de 2,75 m de altura'. Peço respeitosamente que sua prestigiosa instituição investigue esses relatos. Espero ainda que possam averiguar se essas 'criaturas estranhas' (caso realmente existam) estão de algum modo ligadas aos experimentos com DNA recombinante em andamento na região da Nova Inglaterra".
Seguiu-se uma caça às bruxas que praticamente impedia o trabalho na região da Nova Inglaterra, tanto assim que Walter Gilbert, fundador da Biogen, teve que fazer seus experimentos de clonagem do gene de insulina em bactérias num laboratório P4 em Porton Down no sul da Inglaterra, de propriedade do exército britânico. Um outro grupo que competia com Gilbert, formado por Stanley Cohen e Herbert Boyer, fundou em 1976 a Genentech, Genetic Engineering Technology, instalada na Califórnia, onde se respirava um ar de liberdade empreendedora. Eles também escolheram o gene da insulina humana para clonar em bactéria e, embora tivessem optado por uma rota mais complicada que Gilbert, obtiveram o produto muito antes. Sorte dos diabéticos, que até então tomavam injeções de insulina de porco, que difere da insulina em um aminoácido, ou de boi, com 3 aminoácidos de diferença num total de 51 aminoácidos. Apesar de muito semelhantes à insulina humana, com o tempo o organismo desenvolve anticorpos que rejeitam a insulina estranha injetada.
Quando se trata de alimentos, a Europa sempre foi conservadora. Basta relatar a história do tomate. Essa fruta era consumida pelas populações da América pré-colombiana. Levada à Europa ainda no século XVI pelas expedições que retornavam, foi considerada um veneno e somente passou a ser consumida na alimentação na Espanha e na Itália no fim do século XVII. Somente no século XIX o tomate foi plenamente aceito na Europa Central. Não é de surpreender a resistência que eles manifestam contra os alimentos geneticamente modificados.
O PRINCÍPIO DA PRECAUÇÃO
O princípio da precaução apareceu primeiro no direito germânico como reação a acidentes globais em consequência de novas tecnologias que não haviam antecipado danos: mercúrio em alimentos ou água, substâncias tóxicas lançadas ao mar, buraco de ozônio causado por CFC, dentre outros.
O princípio da precaução foi introduzido na Europa na década de 80, tornando-se a base do acordo de 1987, que proíbe o lançamento de substâncias tóxicas persistentes no Mar do Norte. Ele consta da Convenção sobre a Biodiversidade. Um número cada vez maior de leis ambientais suecas e alemãs fundamenta-se no princípio da precaução. Conferências internacionais sobre substâncias tóxicas persistentes e o buraco de ozônio constituíram fóruns para a promoção e debate do princípio da precaução.
Na Conferência Rio 92 - Convenção sobre Diversidade Biológica, o princípio da precaução, Princípio 15, foi proposto formalmente com o seguinte introito: de modo a proteger o meio ambiente, o princípio da precaução deve ser amplamente observado pelos estados, de acordo com as suas capacidades. A sua definição, datada de 14 de junho de 1992, foi a seguinte:
"Quando houver ameaça de danos sérios ou irreversíveis, a ausência de absoluta certeza científica não deve ser utilizada como razão para postergar medidas eficazes e economicamente viáveis para prevenir a degradação ambiental".
"O Princípio da Precaução é a garantia contra os riscos potenciais que, de acordo com o estado atual do conhecimento, não podem ser ainda identificados".
Ora, esse princípio refere-se à "absoluta certeza científica", o que de pronto afasta qualquer possibilidade de discussão porque a ciência, ao contrário do que pensa a maioria, nunca tem absoluta certeza (Van den Belt, 2003). A ciência observa fatos, levanta hipóteses, reúne dados e afirma que determinado fenômeno ocorre com alguma probabilidade, que pode ser baixa ou alta. Quando sobrevêm novos fatos, mudam as conclusões.
Em outras palavras, o princípio da precaução exige certeza científica da ausência de risco, mas risco igual a zero não existe. Dificilmente se consegue identificar uma atividade humana sem risco.
Interpretações desse princípio variam, mas a Declaração de Wingspread (1998) é a primeira que introduz alguma racionalidade na definição, já que admite que o princípio deve ser aplicado quando existe alguma evidência de risco.
"Quando uma atividade representa ameaças de danos ao meio ambiente ou à saúde humana, medidas de precaução devem ser tomadas, mesmo se algumas relações de causa e efeito não forem plenamente estabelecidas cientificamente."
Mas o que seria "risco"? A melhor definição é a que diz que "risco é função da probabilidade de ocorrência de efeito adverso, bem como da severidade desse efeito".
A morte pela varíola nos sessenta anos de proibição da vacina e a guerra da vacina contra a febre amarela no Rio de Janeiro, no início do século passado, são exemplos de que a aplicação do princípio da precaução (embora ainda não tivesse sido formulado) pode produzir danos. Ainda hoje há pessoas que alegam serem as vacinas muito perigosas. Bastaria essa alegação para suspender a aplicação de vacinas nas crianças? A volta do uso de estrume como adubo pode contaminar alimentos com Claviceps purpúrea, que produz ergotamina, Fusarium, que produz fumonisina, e Escherichia coli O157:H7, que produz toxinas. Ainda assim, a agricultura orgânica é um nicho de mercado florescente e ninguém invoca o princípio da precaução contra alimentos orgânicos.
Análises como essa levaram a Comissão Europeia (2000) a concluir que o princípio da precaução serve para gerenciar riscos, mas não para avaliá-los.
Em suma, não basta uma histeria qualquer para invocar o princípio da precaução e paralisar o progresso. Se não fosse assim, alguns poderiam achar que comer alface representasse uma ameaça à saúde humana e, por precaução, todos deveriam deixar de comê-la e medidas de precaução teriam que ser tomadas, ainda que não se soubesse bem se alface faz mal mesmo.
A LEI DE BIOSSEGURANÇA (11.105/05)
Como foi dito no início deste artigo, até março de 2005, as normas de segurança e uso da biotecnologia no Brasil eram estabelecidas pela Lei 8.974/95. Em virtude dos numerosos questionamentos judiciais com relação à referida lei, principalmente porque não se sabia a quem cabia a palavra final em matéria de transgênicos, CTNBio, Ibama, Anvisa, e outros, em 2003, o governo federal enviou ao Congresso Nacional projeto de uma nova lei de biossegurança.
O projeto de lei de nº 2.401/03 tramitou no Congresso Nacional por dois anos e, em 2005, foi definitivamente aprovado pelas duas casas (Câmara e Senado), convertendo-se finalmente na Lei 11.105/05, que atualmente estabelece normas de segurança e mecanismos de fiscalização de atividades que envolvam organismos geneticamente modificados - OGM e seus derivados, cria o Conselho Nacional de Biossegurança - CNBS, reestrutura a Comissão Técnica Nacional de Biossegurança - CTNBio e dispõe sobre a Política Nacional de Biossegurança - PNB.
Regulamentada pelo Decreto 5.591/05, a Lei 11.105/05 estabelece de forma clara que compete à CTNBio a análise técnica da biossegurança do OGM sob o aspecto de saúde humana, vegetal, animal e ambiental, sendo sua decisão técnica vinculante aos demais órgãos fiscalizadores, quais sejam, Ministério da Agricultura, Ministério do Meio Ambiente e Anvisa. Estabelece ainda que compete à CTNBio definir quais atividades com OGM são potencialmente causadoras de significativa degradação ambiental e consequentemente necessitam de licenciamento ambiental.
Vale observar que ao modificar a descrição do Código 20 do Anexo VIII da Lei 6.938/81 (Lei do Meio Ambiente), estabelecendo que a introdução de espécies geneticamente modificadas e o uso da diversidade biológica pela biotecnologia só poderão ser considerados causadores de degradação ambiental se assim identificados pela CTNBio, a nova lei harmonizou a legislação de biossegurança e de meio ambiente e tornou inequívoco o método de análise ao qual deve ser submetido o OGM, qual seja, o método de análise "caso a caso", com o poder vinculante da decisão técnica sobre a biossegurança do OGM emanada da CTNBio sobre os demais órgãos fiscalizadores, elidindo assim o maior motivo dos conflitos jurídicos existentes com relação à Lei 8.974/95.
Outra importante modificação trazida pela Lei 11.105/05 foi definir claramente que não se aplica aos OGMs e seus derivados o disposto na Lei 7.802/1989 (Lei de Agrotóxicos), exceto para os casos em que eles sejam desenvolvidos para servir de matéria-prima para a produção de agrotóxicos, resolvendo desse modo o conflito de normas existente entre a lei anterior e a lei de agrotóxicos.
Outra modificação também trazida pela Lei 11.105/05 foi a criação do Conselho Nacional de Biossegurança - CNBS, ao qual caberá, em casos de liberação comercial de OGM e derivados, analisar, a pedido da CTNBio, os aspectos de conveniência e oportunidade econômicas daquela liberação, bem como avocar de decidir em última instância os recursos dos órgãos fiscalizadores em liberações comerciais de OGM e derivados.
No tocante à rotulagem, estabeleceu em seu artigo 40 que os alimentos destinados ao consumo humano e animal que contenham ou sejam produzidos a partir de OGM ou derivados deverão conter essa informação no rótulo, conforme regulamento.
E, por fim, vedou a utilização, a comercialização, o registro, o patenteamento e o licenciamento de tecnologias genéticas de restrição do uso. Para os efeitos da lei, entende-se por tecnologia genética de restrição do uso qualquer processo de intervenção humana para geração ou multiplicação de plantas geneticamente modificadas que produzam estruturas reprodutivas estéreis, bem como qualquer forma de manipulação genética que vise à ativação ou desativação de genes relacionados à fertilidade das plantas por indutores químicos externos.
Essa última restrição foi introduzida por pressão das entidades ambientalistas preocupadas com a possibilidade de que as grandes multinacionais pudessem esterilizar sementes, vedando o seu uso, largamente utilizado por pequenos agricultores, no ano subsequente à colheita. Na verdade, para grandes árvores, as tecnologias de restrição de uso seriam úteis a fim de evitar que insetos transportassem sementes para outros locais com o consequente crescimento de árvores fora de controle. Como sempre, dispositivos legais estritos que não permitem flexibilidade são contraproducentes. Se há uma comissão para analisar a liberação de OGMs caso a caso por que não deixar à sua discrição as decisões sobre esse assunto?
AS ATRIBUIÇÕES E A COMPOSIÇÃO DA CTNBIO
A CTNBio, portanto, faz análises de risco, ambiental e à saúde humana e animal, de organismos geneticamente modificados (OGMs ou transgênicos). A liberação de sementes para plantio ou produtos veterinários é atribuição do Ministério da Agricultura, Pecuária e Abastecimento e, de produtos para uso na saúde humana, do Ministério da Saúde. Por isso, não é a CTNBio que libera um produto, ela apenas conclui, após exaustivas análises científicas, com fundamento em trabalhos internacionais publicados e em pareceres de especialistas, sobre a probabilidade de risco de liberação comercial de OGMs.
Qual a legitimidade da CTNBio para fazer análises de risco? Para isso, temos que avaliar a sua composição. Ela é formada por 27 membros titulares e 27 membros suplentes, todos com o título de doutor. Muito embora os membros suplentes somente votem na ausência do titular, não é infrequente que, nas reuniões, o suplente esteja presente, ainda que o titular também esteja. Ademais, a lei exige a presença de todos sob pena de exclusão após 3 faltas consecutivas não justificadas. Por isso, tipicamente, em cada reunião estão presentes de 32 a 38 membros, mas somente 27 podem votar. É óbvio que as pessoas mais indicadas para emitir pareceres técnicos na análise de riscos de uso de transgênicos são especialistas em ambiente, agronomia, biologia molecular, bioquímica, medicina, nutrição humana e animal, genética humana, animal e vegetal, microbiologia, dentre outras. E a razão é simples: cada um deles conhece profundamente o funcionamento dos genes, a síntese das proteínas por eles codificadas, a digestão e a absorção de nutrientes, o papel das bactérias e vírus, as formas de interação entre os seres vivos.
Portanto, o ministro da Ciência e Tecnologia nomeia diretamente 13 membros titulares (mais 13 suplentes) ouvindo as sociedades científicas. O ministro Sérgio Machado Rezende, que teve a responsabilidade de instalar a nova CTNBio a partir de fevereiro de 2006, solicitou nomes de cientistas para a Academia Brasileira de Ciências (ABC) e para a Sociedade Brasileira para o Progresso da Ciência (SBPC). Das numerosas sugestões de cientistas, em geral trabalhando em universidades e institutos de pesquisa, o ministro nomeia três de cada área, vegetal, ambiental, saúde humana e saúde animal, além de um 13º membro, que o representa na Comissão. Os demais membros são indicados por outros ministérios, a saber: Meio Ambiente (MMA), Agricultura, Pecuária e Abastecimento (Mapa), Desenvolvimento, Indústria e Comércio (MDIC), Saúde (MS), Justiça (MJ), Trabalho (MT), Defesa (MD), Relações Exteriores (MRE) e Desenvolvimento Agrário (MDA).
ANÁLISES DE RISCO
As análises de risco são feitas com base em experimentos feitos pela empresa interessada em laboratório e em liberação planejada e contida no ambiente, além de trabalhos científicos de abrangência internacional e de pareceres solicitados pela CTNBio a pesquisadores especialistas, atuantes nas universidades e institutos de pesquisa. É evidente que todos os produtos que provêm de organismos geneticamente modificados têm que, obrigatoriamente, ser analisados pela Comissão. No entanto, até o momento, são poucos os produtos destinados à saúde que são fabricados, desde o início, no Brasil. Eles são todos importados, à exceção de alguns como a vacina de hepatite B, produzida no Instituto Butantan por uma levedura geneticamente modificada. A maior parte do trabalho da CTNBio, portanto, além da autorização de projetos de pesquisa nas universidades e institutos de pesquisa, se resume a analisar riscos do plantio em larga escala, para fins comerciais, de soja, milho e algodão geneticamente modificados. Por isso, neste artigo, que tem por finalidade discutir o sistema regulatório de controle de organismos geneticamente modificados, apresentaremos, à guisa de exemplo, os processos de liberação desses produtos.
As análises focalizam duas vertentes: possíveis danos ao ambiente e à saúde humana ou animal. Genericamente são feitas as seguintes perguntas:
1) Efeito adverso: qual o dano?
2) Riscos: como pode aparecer o dano?
3) Riscos significativos: quais riscos, dentre todos, devem ser detalhadamente analisados?
4) Avaliação: como o risco identificado será observado e medido?
O processo de decisão está esquematizado na Figura 1.
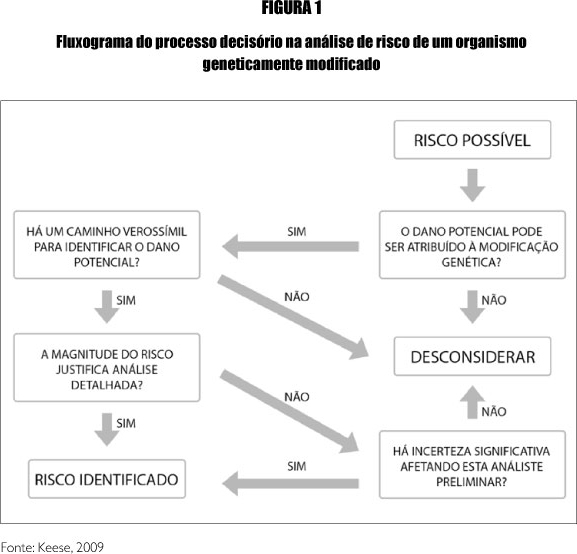
Fonte: Keese, 2009
RISCOS AO AMBIENTE
Preconiza-se o uso da abordagem escalonada (tiered approach), desenhada para identificar áreas de grande preocupação ecológica, pela qual se estabelece uma clara hipótese de risco que é verificada no escalão 1 (tier 1). Caso o produto não passe nesse nível, avança-se para o escalão 2, 3 e 4, sucessivamente, este último referindo-se à liberação em campo aberto (Figura 2). Essa abordagem, baseada em considerações teóricas conhecidas como formulação de problemas (Raybould, 2006), é interessante porque envolve o famoso caso das borboletas monarca, que provocou nervosismo mundial quando se demonstrou que a proteína Cry1Ab, expressa pelo milho Bt, era tóxica para as larvas dessas borboletas, um ícone da biodiversidade no Hemisfério Norte. As lepidopteras-alvo, no caso do milho, são a lagarta-do-cartucho, Spodoptera frugiperda, a lagarta da espiga, Helicoverpa zea, e a lagarta do colmo, Diatrea saccharalis. Sendo a monarca uma lepidóptera, a borboleta tem o receptor para essa proteína em seu intestino e por isso morre como morrem os insetos-alvo, as lagartas que comem as folhas de plantas de milho, soja e algodão, dentre outros. Mas morre quando se força a borboleta a ingerir a proteína. Em campo aberto, uma cultura de milho e a borboleta monarca são estranhos um ao outro porque a lagarta dessa borboleta não se alimenta de milho, soja, algodão e outros. Por isso, no escalão 4 demonstrou-se que o milho transgênico nada faz ao ciclo de vida dessa borboleta. Vários trabalhos estatísticos mostraram que o ciclo de vida da borboleta monarca, do nascimento à morte, é o mesmo longe ou perto de um campo de sementes transgênicas.

O esquema mostra o processo de abordagem escalonada (tiered approach) pela qual, quando uma proteína geneticamente modificada não passa no primeiro escalão, ela é imediatamente examinada no escalão seguinte até a eliminação da expectativa de risco no caso real.
Nos exaustivos estudos de impacto ambiental que a CTNBio exige dos proponentes da nova tecnologia em experimentos contidos no meio ambiente, incluem-se:
• os potenciais efeitos adversos em organismos não alvo como inimigos naturais, quando for o caso, do organismo que está sendo introduzido, nos insetos em geral, nos polinizadores, nos que participam da decomposição da matéria orgânica, nos pássaros e nos roedores e outros animais do entorno;
• a possibilidade de fluxo gênico para espécies sexualmente compatíveis e a improvável transferência horizontal para organismos filogeneticamente distantes; caso a última hipótese fosse fato comum, isto é, a transferência do DNA de uma espécie para outra, os seres humanos que comem vegetais já estariam todos verdes, pois teriam incorporado os genes de síntese de clorofila, por exemplo; igualmente, não há evidências de que o DNA da planta que cai no solo seja incorporado por bactérias e outros microrganismos;
• os efeitos adversos à microbiota do solo, isto é, a proteína produzida pelo gene que foi introduzido no vegetal teria efeito negativo aos micro-organismos do solo?
• o acompanhamento do desenvolvimento de resistência, já que o uso repetitivo de um inseticida ou herbicida poderia selecionar insetos resistentes; nesse caso recomenda-se sempre aos agricultores plantarem uma proporção do mesmo vegetal não modificado para servir de zona de refúgio, exigindo-se um monitoramento, após o plantio, por pelo menos cinco anos.
Fala-se muito em transferência horizontal de genes. Isso existe entre bactérias, nos fenômenos da conjugação e da transformação e na transferência de elementos extracromossomais. Existe, por exemplo, com Agrobacter sp., que infecta tecidos vegetais e transfere de forma integrativa parte de seu material genético para o genoma da planta. Esse material produz hormônios vegetais (auxinas e citocininas) e opinas (nopalina, ocotopina, agropina e miquimopina, dentre outras), desequilibrando o balanço hormonal e provocando multiplicação incontrolada das células infectadas gerando um tumor na planta. Foi essa capacidade da bactéria que, retirados todos esses genes, mas mantidos os que permitem a infecção, foi aproveitada para a realização da primeira transformação genética em plantas, pois a propriedade da bactéria de inocular genes na célula hospedeira foi usada para introduzir um gene de interesse.
Todos os alimentos contêm DNA, que é ingerido em quantidades significativas. No homem, o consumo pela dieta de RNA e DNA, embora variado, está na faixa de 0,1 a 1 g por dia, isso sem contar com o fabuloso número de 150.000.000 de bactérias (e seu DNA) por mg de fezes humanas, o que corresponde a 2/3 do peso das fezes secas. Qualquer preocupação sobre a presença de novo DNA em um alimento geneticamente modificado, consumido na dieta humana, tem que levar em conta que esse DNA representa menos que 1/250.000 da quantidade de DNA consumido. Os organismos vivos podem ter 50.000 genes, que são apenas uma fração da quantidade total de DNA. A inserção de um gene numa célula talvez aumente a quantidade de DNA em 1/1.000.000 ou menos. Essa inserção provoca um efeito muito importante, social e econômico, mas não altera a biologia do organismo.
Além disso, a probabilidade de transferência de genes de plantas geneticamente modificadas para células de mamíferos é extremamente baixa, como também é extremamente baixa a probabilidade de transferência de DNA da planta para microrganismos (Malarkey, 2003). Experimentos destinados a essa finalidade, em condições excepcionais que não as naturais, dão frequências de 10-17 a 10-20, isto é, de 1 vez para 1 quintilhão para 1 sextilhão de vezes. Uma excelente revisão nessa área é a de Keese (2008).
No caso da transmissão vertical, temos que analisar se a planta é autógama - quando há predominância de autopolinização - ou alógama quando há predominância de polinização cruzada. Na autógama, o pólen de uma flor é transferido para o estigma da mesma flor ou de flor da mesma planta: feijão, amendoim, tomate, soja, trigo, batata, arroz, alface e cevada. Na alógama, o pólen de uma flor é transferido para o estigma de uma flor de outra planta, onde ocorre a fecundação: cacau, girassol, eucalipto, milho, mamão, mandioca, beterraba, uva e goiaba. Nessas a fecundação cruzada é maior que 90%. Há ainda as intermediárias, com 5% a 50% de taxa de fecundação cruzada, como algodão, canola e berinjela. Finalmente, há as que também têm reprodução assexuada porque podem se propagar através de bulbos, rizomas, caules e tubérculos: cana-de-açúcar, batata, mandioca, morango e banana.
Para haver fluxo gênico de uma planta para outra é necessário que: 1) as plantas sejam sexualmente compatíveis; 2) se desenvolvam no mesmo ambiente; 3) tenham período comum de florescimento; 4) haja uma forma de transporte do pólen.
Nesse caso, quando há esse risco estabelecem-se regras de coexistência e monitoramento. Trabalhos exaustivos de Paterniani, Patto Ramalho e outros mostram que uma distância de 20 metros entre duas plantações de milho pode dar fecundação cruzada com taxa menor que 1%. Por isso, a CTNBio determinou para coexistência uma zona tampão de 100 metros ou 20 metros com adicionais 10 linhas de bordadura de milho convencional (cf. Andrade et al., 2009). De qualquer modo, há que considerar que, não havendo pressão seletiva, o contaminante irá eventualmente desaparecer, já que a sobrevivência está relacionada com a vantagem competitiva. O manejo e a rotação de culturas têm-se revelado importantes para evitar o fluxo gênico vertical.
Nos últimos quatro anos, a CTNBio foi extremamente castigada pela insistência de membros do Ministério Público em exigir a execução de EIA/Rima (estudo e relatório de impacto ambiental), que é uma exigência para grandes construções que provocam graves impactos no ambiente como, por exemplo, a construção de grandes barragens e usinas geradoras de energia. Nesse caso, o estudo tem que ser prévio e deve estimar quantas árvores serão submersas, quantos animais do ecossistema serão prejudicados, o que irá acontecer com os pássaros que migram pelo local, dentre outros. A Lei de Biossegurança dispõe que a CTNBio deve avaliar se é ou não necessário fazer EIA/Rima.
É necessário enfatizar que um campo de milho transgênico provoca exatamente o mesmo impacto ambiental que um campo de milho não transgênico. Algum impacto sempre há, mas é o impacto da agricultura, já que, desde que o homem domesticou plantas para seu uso, ele provocou necessariamente algum dano ao ambiente original. Por isso, os estudos com as liberações contidas no meio ambiente são suficientes para aquilatar a segurança do plantio do organismo transgênico. Seria absurdo se fôssemos exigir dos agricultores obter aprovação de um EIA/Rima para plantar qualquer coisa!
RISCOS À SEGURANÇA ALIMENTAR
Quanto à questão da segurança alimentar, os produtos geneticamente modificados devem ser rigorosamente avaliados antes de serem lançados no mercado. Um dos problemas é sua alergenicidade potencial. Esse aspecto é muito caro à indústria de alimentos. Por esse motivo, é imperativo evitar que um gene transferido codifique uma proteína alergênica em alimento anteriormente isento dessa propriedade (Codex alimentarius). A Comissão do Codex Alimentarius (http://www.who.int/foodsafety/codex/en/), cujas instruções são seguidas pela CTNBio, foi criada em 1963 pela FAO (Food and Agriculture Organization, órgão da ONU) e pela OMS (Organização Mundial da Saúde) para desenvolver regras quanto à produção e uso de alimentos. Para isso, desenvolveu-se um Programa Conjunto FAO/OMS de Padrões Alimentares cujas finalidades principais são proteger a saúde dos consumidores e assegurar práticas comerciais justas, além de promover coordenação de todos os trabalhos relacionados e desenvolvidos por organizações governamentais e não governamentais nessa área.
O problema da alergia deve ser colocado na perspectiva correta. Estima-se que ela ocorra com a frequência de 6% em crianças pequenas e 3% em adultos. Amendoins e camarões nunca foram banidos do mercado apesar de 1% da população poder desenvolver reações alérgicas à exposição a esses alimentos. Kiwi, que foi introduzido recentemente, desencadeou novos episódios de alergia. É impensável banir a comercialização de frutas ou alimentos que afetam apenas 1% da população, mas deve-se alertar por todos os meios essa possibilidade. Esse mesmo argumento pode ser usado para cultivos geneticamente modificados.
Até o momento, não se conhecem efeitos alergênicos dos alimentos geneticamente modificados. O alerta, entretanto, existe porque houve um caso bem no início de desenvolvimento dessa tecnologia e que, talvez, tenha contribuído para uma certa rejeição desses produtos. A ideia, em 1996, foi introduzir na soja o gene de albumina 2S da castanha-do-pará para aumentar o teor de metionina na soja a fim de enriquecer o poder nutricional de alimentos para animais. Até o momento, não havia indicações de que essa proteína fosse alergênica, mas estudos conduzidos durante o desenvolvimento do produto demonstraram ligação com IgE (imunoglobulina E) de soros de brasileiros alérgicos a castanha-do-pará, além de reações positivas em testes cutâneos conduzidos com a proteína. Essa proteína é conhecida agora como o alérgeno mais importante da castanha-do-pará. É necessário enfatizar que não foi o produto transgênico o responsável pela alergia, mas a proteína original da castanha-do-pará, cujas propriedades alergênicas eram desconhecidas. Por isso, as instruções do Codex enfatizam que é importante e mais eficiente proceder a uma avaliação antes da comercialização do que a uma análise posterior (cf. Goodman et al., 2008).
O ponto de partida é o da equivalência substancial, que é um conceito usado para identificar semelhanças e diferenças entre o alimento geneticamente modificado e um comparador histórico de uso seguro como alimento, para guiar processos subsequentes de avaliação de risco. Houve e há muitas críticas a esse conceito porque ele foi tomado como um ponto final de avaliação e, na verdade, ele é apenas ponto de partida, mas que oferece evidência robusta e garante tranquilidade. Em outras palavras, o princípio da equivalência substancial compara a composição de um alimento transgênico com a mesma variedade não transgênica.
Assim, antes de liberar uma planta para uso comercial é necessário avaliar os riscos a fim de desenvolver uma estratégia de gerenciamento desses riscos: 1) reprovação; 2) aprovação com rotulagem invocando precaução ou com monitoramento; 3) aprovação sem restrições. É evidente que em alguns casos pode-se amealhar informação preexistente e, em outros, é fundamental realizar experimentos.
As proteínas são constantemente sintetizadas e degradadas no organismo. O corpo humano sintetiza aproximadamente 300 g de proteínas novas por dia. Para isso, um organismo tem necessidade de um suprimento constante de aminoácidos que provêm das proteínas que ele ingere, em torno de 100 g por dia. O resto ele obtém dele mesmo, digerindo a mucosa gastrointestinal descamada (35-200 g de aminoácidos por dia).
As proteínas são grandes moléculas formadas pela reação, entre si, de 20 aminoácidos obtidos na alimentação pela ingestão de proteínas animais ou vegetais. As ligações químicas entre os aminoácidos são denominadas ligações peptídicas. Para fornecer esses aminoácidos, as proteínas ingeridas têm que ser degradadas, e a degradação é exatamente pela ruptura das ligações peptídicas que ligam um aminoácido ao outro. É como se, para construir uma nova parede de tijolos, derrubássemos outra, de forma cuidadosa, para obter esses tijolos. A degradação das proteínas no estômago dos mamíferos começa imediatamente após a ingestão, em meio altamente ácido que destrói a estrutura espacial tridimensional da proteína e permite a ação da enzima pepsina, que cliva a proteína em várias ligações peptídicas. Essa digestão continua no intestino delgado por tripsina, quimotripsina, leucilaminopeptidases, carboxipeptidases, dentre outras, até que toda a proteína se converta em seus aminoácidos constituintes, finalmente absorvidos.
Quando não se sabia o destino das proteínas no sistema digestivo pensava-se que era possível administrar insulina ou hormônio de crescimento via oral. Agora sabemos que isso é impossível já que praticamente todas as proteínas são digeridas e não alcançam as fezes excretadas. Há, entretanto, algumas proteínas que são absorvidas intactas e por isso, no caso dos transgênicos, caso a caso, por precaução, deve-se estudar se isso acontece. Para todos os transgênicos já liberados para plantio as proteínas introduzidas são completamente digeridas, isto é, as proteínas transgênicas são destruídas em minutos no estômago e no intestino.
No entanto, existem algumas proteínas que representam perigo quando ingeridas. Algumas são toxinas e outras, antinutrientes como as lectinas (Tabela 1). Por exemplo, a cepa altamente virulenta de E. coli O157:H7 produz enterotoxina que ataca a mucosa intestinal causando citotoxicidade direta. Essa bactéria contamina com frequência alimentos orgânicos que são adubados com estrume. Outras proteínas como as lectinas que existem no feijão somente são destruídas se cozidas. Se comêssemos feijão cru, essas proteínas não seriam digeridas no estômago e se ligariam a carboidratos das membranas celulares perturbando a digestão (Tabela 1). As proteínas transgênicas são, pois, comparadas em bancos de dados com essas proteínas tóxicas para afastar a possibilidade de ocorrência de segmentos homólogos de aminoácidos.

Toda proteína transgênica introduzida em plantas tem sua sequência comparada com as sequências das toxinas nos bancos de dados a fim de afastar a possibilidade de semelhanças em segmentos da proteína.
Quanto à alergenicidade podemos afirmar que pouquíssimas proteínas alimentares são alergênicas, mas todos os alérgenos na comida são proteínas. Aqui se usa o sistema do peso da evidência caso a caso: histórico de uso, análise bioinformática, comparando a sequência de aminoácidos com alérgenos conhecidos e estabilidade da proteína à ação da pepsina in vitro. Caso nesses testes haja dúvida quanto à segurança, é necessário passar a testes toxicológicos usando ratos e camundongos, verificando ligação a anticorpos IgE de pessoas alérgicas e perfazendo experimentos clínicos. No entanto, se uma proteína transgênica ligar-se a anticorpos IgE de pessoas alérgicas ela estará condenada para liberação comercial.
Na avaliação de risco do uso de alimentos transgênicos temos que proceder à identificação do perigo potencial e à caracterização do perigo. No perigo potencial avaliamos:
1) o histórico de uso seguro: os países do norte da América do Norte vêm usando alimentos transgênicos desde 1995 sem relato algum de efeitos adversos. Esse fato deve ser levado em conta, ainda que não como critério único, porque populações com diferentes hábitos culturais vivendo em diferentes regiões geográficas podem ter sido expostas a antígenos sensibilizadores que cruzam com a proteína transgênica;
2) o modo de ação: por exemplo, as proteínas Cry de Bacillus thuringiensis, que naturalmente é um inimigo de lepidoptera (lagarta do cartucho), diptera (moscas) e coleoptera (besouros), a depender da especificidade das quase 200 proteínas Cry sintetizadas por essa bactéria. A agricultura orgânica permite o uso dessa bactéria, cujos esporos são lançados diretamente sobre as plantas para combater o ataque das lagartas (um estágio do desenvolvimento das lepidoptera - borboletas - que atacam a maioria das plantas). O gene de uma proteína Cry é introduzido em milho ou algodão e as plantas ficam protegidas do ataque dessas pragas. As proteínas Cry, quando ingeridas pela lagarta, são clivadas gerando um fragmento que é reconhecido por um receptor na superfície do epitélio intestinal da lagarta. A interação do fragmento de proteína Cry com o receptor rompe a membrana intestinal e acaba por matar a lagarta. Pois bem, somente as lagartas de lepidoptera possuem o receptor e por isso as proteínas Cry não induzem ruptura de membrana de qualquer outro animal, inclusive o homem;
3) alguns antígenos alergênicos têm se-quências de 6 a 8 aminoácidos que se repetem entre os alérgenos. Ainda aqui deve-se ter cautela porque nem sempre a presença dessas sequências transforma uma proteína em alergênica e nem é necessário a presença dessas sequências para que uma dada proteína seja alergênica. Não obstante, a sequência de aminoácidos das proteínas transgênicas é comparada em banco de dados com as sequências de aminoácidos de proteínas reconhecidamente alergênicas;
4) digestibilidade e estabilidade in vitro: experimentos são feitos in vitro na presença das condições que a proteína encontrará no estômago do ser humano, medindo-se o tempo que o suco gástrico leva para destruir a proteína, já que o ambiente ácido em conjunto com a enzima pepsina destrói as ligações peptídicas. É fácil entender que uma proteína transgênica que é destruída em poucos minutos tem pequeníssima probabilidade de induzir a formação de anticorpos no intestino;
5) níveis de expressão na planta e de consumo na dieta: em todos os casos sabe-se perfeitamente onde a proteína é expressa na planta e em que quantidade. Por exemplo, muitas vezes os níveis de expressão nas folhas e no caule, que são atacados pelas lagartas, são muito maiores do que nos grãos. A quantificação dessa expressão nos dá uma ideia da quantidade de ingestão da proteína em questão.
Quanto à caracterização do perigo, que é uma fase mais avançada da abordagem escalonada que devemos adotar, fazemos estudos de toxicologia aguda em animais, administrando por gavagem (introdução direta forçada pela boca do animal) as proteínas purificadas que queremos estudar (Tabela 2). As quantidades experimentadas são enormes para o peso dos animais e absolutamente irreais. Nas quantidades utilizadas nada aconteceu aos animais. Ainda assim, se houver dúvidas restantes pode-se fazer estudos de toxicologia por doses repetidas e, finalmente, avaliação caso a caso baseada em hipóteses. No entanto, se as dúvidas persistirem até este ponto, é melhor não liberar o produto.

As doses máximas utilizadas não provocaram efeito algum em camundongos
Em resumo, são os seguintes os procedimentos para garantir segurança alimentar:
1) evitar introduzir genes que codificam alérgenos em plantas sem história de alergenicidade;
2) se a fonte do gene é um alimento comumente alergênico ou se a proteína contiver sequências de aminoácidos com grande identidade com sequências de proteínas alergênicas, ela deverá ser avaliada quanto à capacidade de ligação com IgE de soros de pacientes alérgicos à fonte doadora do gene ou às sequências peptídicas coincidentes (número suficiente para estatísticas com 95% de confiança);
3) resistência da proteína à digestão por pepsina, presumindo-se que há maior probabilidade de aparecimento de reações alérgicas com proteínas que são pouco digeridas, isto é, elas são fatores de risco para a indução de novas alergias.
APROVAÇÃO DE ORGANISMOS GENETICAMENTE MODIFICADOS NO BRASIL
Quando a nova CTNBio se instalou, em fevereiro de 2006, em decorrência da Lei 11.105/05 e do Decreto 5.591/05, promulgado em novembro de 2005, havia apenas dois organismos geneticamente modificados liberados para uso comercial. O primeiro foi a soja RR já mencionada, cuja liberação comercial foi suspensa por decisão judicial, e o segundo foi o algodão BollGard, aprovado em março de 2005, ao apagar das luzes da CTNBio antiga, que foi dissolvida pela promulgação da Lei de Biossegurança em 24/3/2005. Havia ainda duas vacinas transgênicas aprovadas para uso em animais.
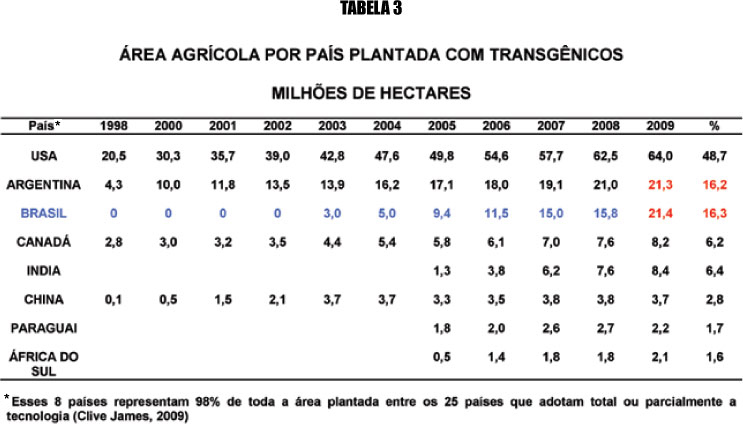
A proibição judicial impôs um atraso na agricultura brasileira considerável deixando o país atrás da Argentina, país vizinho que nunca enfrentou os problemas de oposição que existem no Brasil. A Tabela 3 - cujos dados são extraídos de uma publicação anual de Clive James, presidente do Conselho do Serviço Internacional para Aquisição de Aplicações em Agrobiotecnologia (ISAAA), que teve como patrocinador-fundador Norman Borlaug, o homem da revolução verde, prêmio Nobel - demonstra isso. Na bibliografia citamos a publicação de 2009, mas a tabela foi construída também com informações retiradas de edições de anos anteriores (http://www.isaaa.org). Em 2009, pela primeira vez, o Brasil passou a Argentina em hectares plantados. Nesse ano, um recorde de 14 milhões de agricultores, sendo 90% pequenos agricultores em 25 países, plantaram 134 milhões de hectares de plantas geneticamente modificadas, um aumento sustentável de 7% ou de 9 milhões de hectares quando comparado a 2008 (James, 2009).
Basicamente há dois tipos de alimentos transgênicos: os tolerantes a herbicidas e os resistentes a insetos. Esses últimos resistem aos insetos porque foi introduzido um gene da família Cry de Bacillus thuringiensis (o bacilo é usado inteirinho e jogado em cima das plantas pelos agricultores orgânicos). Dependendo do gene Cry usado (há quase 200 homólogos) a planta resiste a lepidoptera (lagarta do cartucho), coleoptera ou diptera. Essas proteínas encontram receptores específicos no intestino desses insetos e fazem pequenos furos que os matam. Portanto, a proteína estranha nessas plantas (milho, soja, algodão, canola) é a Cry.
Há dois tipos de herbicida: o glifosato, análogo à glicina, e o glufosinato, análogo à homoalanina. Recentemente, a Embrapa clonou o gene de resistência a imidazolinonas em soja. Esse gene foi retirado do arroz que comemos e que apareceu por mutagênese química. O primeiro ficou famoso porque foi introduzido pela Monsanto (tecnologia RR de round up ready) e o segundo pertence à Bayer (tecnologia LL, Liberty Link). No primeiro transgênico introduz-se um gene que faz uma enzima que resiste ao herbicida RR: todas as outras plantas morrem, exceto o transgênico. O glifosato inibe a enzima que está na via do shikimato, precursor dos aminoácidos aromáticos, que não existe nos vertebrados.
No segundo transgênico, introduz-se na planta uma enzima que destrói o herbicida glufosinato que, por sua vez, em plantas sensíveis, inibe a utilização de glutamina. A proteína estranha nesse caso é a PAT ou a BAR, que são acetilases de glufosinato. Evidentemente, por cruzamentos genéticos clássicos entre dois OGMs, pode-se construir uma planta com os dois ou mais genes.
As tabelas 4-7 mostram os tempos de espera entre a submissão do pedido e a aprovação, notando-se claramente que a Lei de Biossegurança funcionou quando posta em prática por uma comissão atuante. Alguns pontos devem ser ressaltados: 1) o evento CV127 foi obtido por engenharia genética realizada inteiramente no Brasil por cientistas da Embrapa/Cenargen usando um gene de propriedade da Basf; 2) produtos da segunda geração de transgênicos já estão sendo analisados e liberados. Esses produtos são obtidos por cruzamento genético clássico entre plantas com características genéticas introduzidas diferentes. Em geral, cruzam-se produtos que ganharam a propriedade de resistir ao ataque de insetos com plantas resistentes a herbicida. Esses produtos são conhecidos como piramidados (stacked, em inglês); 3) a primeira vacina que a nova comissão discutiu destinava-se a porcos para prevenir a doença de Aujeszky; nessa sessão estavam presentes apenas 21 dos 27 votos possíveis e até essa época eram necessários os votos favoráveis de 2/3 dos membros da comissão - 18 votos - para aprovação de qualquer liberação comercial; a vacina recebeu 17 votos favoráveis contra 4 e, consequentemente, não foi aprovada. Esse episódio demonstrou que uma aguerrida oposição poderia bloquear qualquer coisa dentro da comissão. A consequência foi que deputados, com apoio do governo, propuseram a mudança da lei, permitindo que as aprovações exigissem apenas maioria absoluta, isto é, os votos de mais da metade dos membros.
ESTUDOS SOCIOECONÔMICOS
Em extenso trabalho de Brookes & Barfoot (2006) fez-se um estudo de impacto global do uso de plantas geneticamente modificadas entre 1996 e 2005 nos ganhos do agricultor, uso de pesticidas e emissões de gases do efeito estufa. A análise demonstrou que houve efeitos econômicos notáveis para o agricultor, com um total acumulado favorável de US$ 27 bilhões comparado ao que seria ganho se a tecnologia não fosse adotada. Desses, US$ 13 bilhões foram ganhos pelos fazendeiros norte-americanos e US$ 5 bilhões por argentinos. Os agricultores brasileiros tiveram um ganho de apenas US$ 1,4 bilhão tendo em vista que a liberação dos transgênicos foi feita em meados de 2004, embora se admita internacionalmente que o Brasil tenha plantado soja contrabandeada da Argentina desde 1997. A maior parte disso foi ganha por agricultores em países em desenvolvimento. A tecnologia resultou no uso de menos 224 milhões de quilos de pesticida e redução de 15,3% no impacto ambiental associado ao uso de pesticida. Somente no ano de 2005 houve uma redução de emissão de gases do efeito estufa de 9 bilhões de quilos, equivalente à remoção, por ano, de 4 milhões de automóveis das estradas.
TABELA 4
Soja geneticamente modificada. Tempo decorrente entre submissão e aprovação
| Evento | Gene | Característica | Empresa | Submissão | Decisão | Tempo |
| RR MON87701 | epsps
Cry1Ac/epsps | Tolerância a herbicida Resistência a insetos e tolerância a herbicida | Monsanto
Monsanto | 06/1998
06/2009 | 10/1998
08/2010 | 5 meses(1)
14 meses |
(1) essa decisão foi suspensa pela Justiça até 2004.
(2) o produto descrito na última linha já pertence à segunda geração de transgênicos obtida pelo cruzamento por genética clássica de dois transgênicos, um resistente a insetos (gene Cry) e outro tolerante a herbicida (gene epsps)
TABELA 5
Algodão geneticamente modificado. Tempo decorrente entre submissão e aprovação
| Evento | Gene | Característica | Empresa | Submissão | Decisão | Tempo |
| BollGard i | Cry 1Ac | Resistência a insetos | Monsanto | 05/2003 | 03/2005 | 2 anos |
| LL | pat | Tolerância a herbicida | Bayer | 05/2004 | 09/2008 | 4 anos |
| MON 1445 | epsps | Tolerância a herbicida | Monsanto | 09/2004 | 10/2008 | 4 anos |
| Widestrike | Cry1F/Cry1Ac/pat | Resistência a insetos e tolerância a herbicida | Dow | 09/2006 | 03/2009 | 2 ½ anos |
| BollGard II | Cry1Ac/Cry2Ab2 | Resistência a insetos | Monsanto | 06/2007 | 05/2009 | 2 anos |
| MON 531 X MON | Cry1Ac/epsps | Resistência a insetos e tolerância a herbicida | Monsanto | 11/2008 | 10/2009 | 11 meses |
| GHB 614 | 2mepsps | Tolerância a herbicida | Bayer | 03/2010 | 12/2010 | 9 meses |
| T30440/GHB119 | Cry1Ab, Cry2Ae, Bar | Resistência a insetos e tolerância a herbicida | Bayer | 07/2010 | Em análise | - |
| MON88913 | Cp4epsps | Tolerância a herbicida | Monsanto | 08/2010 | Em análise | - |
TABELA 6
Milho geneticamente modificado. Tempo decorrente entre submissão e aprovação
| Evento | Gene | Característica | Empresa | Submissão | Decisão | Tempo |
| BollGard I | Cry 1Ac | resistência a insetos | Monsanto | 05/2003 | 03/2005 | 2 anos |
| LL | pat | tolerância a herbicida | Bayer | 05/2004 | 09/2008 | 4 anos |
| MON 1445 | epsps | tolerância a herbicida | Monsanto | 09/2004 | 10/2008 | 4 anos |
| Widestrike | Cry1F/Cry1Ac/pat | resistência a insetos e tolerância a herbicida | Dow | 09/2006 | 03/2009 | 2 ½ anos |
| BollGard II | Cry1Ac/Cry2Ab2 | resistência a insetos | Monsanto | 06/2007 | 05/2009 | 2 anos |
| MON 531 x MON | Cry1Ac/epsps | resistência a insetos e tolerância a herbicida | Monsanto | 11/2008 | 10/2009 | 11 meses |
| GHB 614 | 2mepsps | tolerância a herbicida | Bayer | 03/2010 | 12/2010 | 9 meses |
| T30440/GHB119 | Cry1Ab, Cry2Ae, Bar | resistência a insetos e tolerância a herbicida | Bayer | 07/2010 | em análise | - |
| MON88913 | Cp4epsps | tolerância a herbicida | Monsanto | 08/2010 | em análise | - |
TABELA 7
Vacinas para uso animal. Tempo decorrente entre submissão e aprovação
| Produto | Característica | Empresa | Submissão | Decisão | Tempo |
| Recombitek | Cães/Viroses | Merial | 02/1988 | 05/1998 | 3 meses |
| Vaxxitek MD/iBD | Aves/Marek-Gumboro | Merial | 11/2003 | 05/2004 | 6 meses |
| PrV Marker | Suinos/aujeszky | Schering | 06/2002 | 11/2006 | 4 anos (*) |
| Suvaxyn PCV2 | Suinos/Circovirose | Fort Dodge | 04/2007 | 03/2008 | 11 meses |
| Ingelvac | Suinos/Circovirose | Boehringer | 05/2007 | 06/2008 | 1 ano |
| P. Circumvent | Suinos/Circovirose | intervet | 02/2008 | 10/2008 | 7 meses |
| Poulvac | Aves/E. coli | Fort Dodge | 02/2009 | 10/2009 | 8 meses |
| Vectormune FP-MG | Aves/roup-Micoplasma | Ceva | 02/2009 | 12/2009 | 10 meses |
| Vectormune FP-MG+ae | Aves/roup-encefalomielite | Ceva | 02/2009 | 12/2009 | 10 meses |
| Vectormune HVt-iBD | Aves/Marek-Gumboro | Ceva | 02/2009 | 02/2010 | 1 ano |
| Vectormune HVt-NDV | Aves/Marek-Newcastle | Ceva | 02/2009 | 02/2010 | 1 ano |
| PouvacSt | Aves/Salmonelose | Fort Dodge | 05/2010 | 11/2010 | 6 meses |
(*) essa vacina foi rejeitada apesar de receber 17 votos a favor e 4 contra. o estranhamento que isso gerou fez com que o Congresso Nacional mudasse o quórum de aprovação para liberações comerciais de 2/3 dos membros para maioria absoluta.
Aprofundado estudo da Céleres (2010) informa que a adoção do algodão BollGard, resistente a insetos, resultou numa redução do uso de água - diretamente relacionada com a aspersão de inseticidas - de 42,5 milhões de litros na colheita 2008-2009. Projeções levam a crer que, se a adoção da tecnologia for mantida na velocidade atual ou maior, o Brasil economizará entre 3 e 4 bilhões de litros de água no período 2009-2010 a 2018-2019. Na colheita 2008-2009, foram economizados 350.000 litros de óleo diesel, o que resultou numa diminuição de 940 toneladas do CO2 lançado na atmosfera. As projeções para a próxima década também indicam uma diminuição de uso de óleo diesel de 25 milhões de litros correspondendo à retirada de circulação de uma frota de 10.000 automóveis no período. Isso significaria uma redução da emissão de 66.000 a 91.000 toneladas de CO2 correspondendo a preservar entre 489.000 - 676.000 árvores. Essa vantagem na adoção de organismos geneticamente modificados é também vista nas culturas de milho e soja no Brasil: menor uso de inseticidas, de água e óleo diesel, bem como menor emissão de gases do efeito estufa.
POSSÍVEIS NOVOS CAMINHOS
1) Produzir OGMs com genes direcionados para absorver o máximo de fertilizante a fim de aumentar os rendimentos na colheita.
2) Produzir substâncias no OGM que reforcem as defesas genéticas naturais contra danos provocados por insetos e contaminação por fungos.
3) Transformar as plantas em organismos mais resistentes ao stress - frio, seca, excesso de sal, calor - que são características expressas por genes encontrados em outras plantas.
4) Melhorar o valor nutricional dos alimentos em direções específicas sem mudar as outras características.
5) Reduzir o uso de pesticidas químicos usando genes que estão à disposição em microrganismos do solo.
6) Reduzir o impacto ambiental do gado introduzindo modificações genéticas no capim a fim de reduzir as emissões de metano.
7) Fornecer alternativas para uso industrial construindo plantas direcionadas a fazer amido, combustíveis, substâncias farmacêuticas, usando apenas a energia solar.
A POSIÇÃO DO VATICANO
Em uma semana de estudos (15-19/5/2009) sobre "Plantas Transgênicas para Segurança Alimentar no Contexto do Desenvolvimento", patrocinados pela Pontifícia Academia de Ciências em sua sede na Casina Pio IV no Vaticano, os participantes reafirmaram as conclusões de documento anterior oriundo de uma sessão de estudo denominada "Plantas Geneticamente Modificadas para Combater a Fome no Mundo" que, em resumo, afirma que a agricultura como praticada atualmente é insustentável pelo uso exagerado de pesticidas e pela erosão maciça do solo e que a aplicação da engenharia genética e outras modernas técnicas moleculares contribui para enfrentar esses desafios. O documento é um manifesto de confiança na comunidade científica mundial e dentre outras coisas ensina (Potrykus & Ammann, 2010):
"Há muitos termos distintos usados para descrever processos envolvidos em cruzamentos de plantas. Todos os organismos vivos são feitos de células nas quais estão contidos os genes que lhes proporcionam características distintivas. O conjunto completo de genes (o genótipo) é contido no DNA e é denominado genoma; é a informação hereditária que é passada dos pais para a descendência. Todo o cruzamento de plantas, e de fato toda a evolução, envolve mudanças genéticas ou modificações seguidas de seleção das características mais benéficas dentre os descendentes. A maioria das alterações do fenótipo ou características observáveis (tais como a estrutura física, o desenvolvimento, as propriedades bioquímicas e nutricionais) resulta de mudanças no genótipo. O cruzamento tradicional de plantas usa o embaralhamento aleatório dos genes entre espécies sexualmente compatíveis ou bastante próximas, frequentemente com consequências imprevisíveis e sempre com os detalhes inexplorados das modificações genéticas. Em meados do século XX isso foi suplementado com mutação, isto é, o tratamento aleatório de sementes ou de plantas com substâncias químicas mutagênicas ou radiação de alta energia na esperança de obter melhoramento fenotípico; isso também leva a consequências genéticas imprevisíveis e também não estudadas: o agricultor selecionava as plantas com características mais convenientes. Mais recentemente, desenvolveram-se técnicas que permitem a transferência de genes específicos, identificados e bem caracterizados, ou pequenos blocos de genes que conferem traços particulares, acompanhada de análise precisa dos resultados genéticos e fenotípicos: esta última categoria é chamada 'transgênese' (pelo fato de que genes são transferidos de um doador a um receptor) ou 'engenharia genética'. No entanto, verdadeiramente, esse termo aplica-se a todos os cruzamentos, qualquer que seja o procedimento usado".
Essa descrição didática do processo de cruzamento genético está esquematizada na Figura 3. A revolução verde que deu o Prêmio Nobel a Norman Borlaug baseou-se em intenso emprego de mutagênese de variedades existentes e cruzamentos entre variedades, com a seleção dos melhores traços. Ainda comemos variedades, como arroz, que foram obtidas dessa forma, por exemplo, o arroz resistente ao herbicida imidazolinona, que elimina, nas plantações, o indesejado arroz vermelho. Pela Figura 3 não há diferença conceitual entre uma variedade convencional obtida por cruzamento clássico e outra que recebeu um transgene com uma determinada característica. A única diferença é que nos cruzamentos clássicos, seja com variedades convencionais ou mutagenisadas, desconhece-se quais genes foram transmitidos, selecionando-se a posteriori a planta com as características desejadas, enquanto no transgênico sabe-se exatamente qual gene foi introduzido e onde ele está.
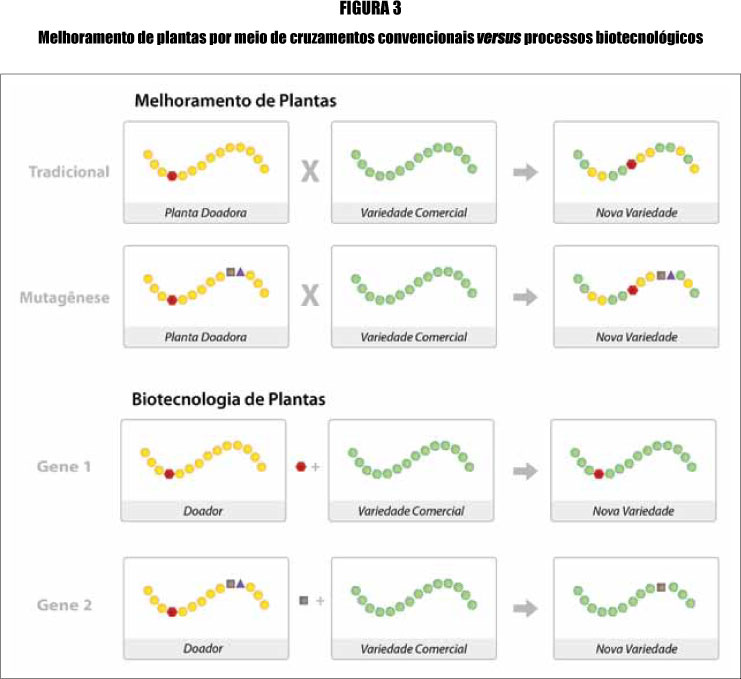
Na tecnologia convencional a planta resultante de um cruzamento entre uma planta doadora e uma variedade comercial possui genes misturados de ambas. Se a planta doadora foi submetida à mutagênese por radiação ou substâncias químicas, seu cruzamento com a variedade comercial igualmente resultará em uma mistura de genes, inclusive os mutados. Esses genes misturados normalmente não são e nunca foram submetidos a regulamentação. Já nos processos biotecnológicos modernos o gene de interesse do doador é isolado em laboratório e introduzido na variedade comercial, resultando em nova variedade que contém somente aquela nova característica, normalmente localizável no genoma (Gene 1). O doador também pode ser um DNA previamente mutado e o gene mutado isolado é introduzido na variedade comercial como no caso anterior (Gene 2). Nesses dois últimos casos há forte regulamentação, embora as novas variedades resultantes sejam facilmente caracterizáveis, ao contrário daquelas obtidas pelos métodos tradicionais.
CONCLUSÃO
As técnicas de engenharia genética introduziram uma revolução na área de medicamentos, vacinas, alimentos e energia. O primeiro transgênico comercializado foi a insulina e logo depois o hormônio de crescimento. Esse último, que era obtido de hipófises de cadáveres, muitas vezes cotransmitia o príon - também uma proteína - que determina a doença de Creutzfeldt-Jakob, a versão humana da doença da vaca louca. A introdução em bactérias dos genes humanos que codificam essas proteínas eliminou vários problemas carreados pelas preparações anteriores, que tinham origem em animais ou seres humanos. Seguiram-se vacinas como a da hepatite B, HPV, e várias vacinas para animais. Muitas enzimas adicionadas ao sabão em pó são proteínas recombinantes, assim como a quimosina usada para a fabricação de queijos, até os franceses. Recentemente, modificações em levedura estão gerando precursores de borracha (isopreno) e óleo diesel (farneseno). As leveduras modificadas serão a base da indústria química futura, pois a fermentação de leveduras transgênicas fornecerá 2, 3, 4, 5 e mais carbonos para sínteses orgânicas. Aos poucos o petróleo será substituído, para esse efeito. Recentemente, a CTNBio aprovou a liberação planejada (contida) de machos do mosquito Aedes aegypti em algumas áreas da região de Juazeiro na Bahia. A linhagem OX513A contém um transgene que produz uma proteína lesiva, em 7 dias, à musculatura do mosquito macho. O promotor (sinal de funcionamento) desse gene é inibido com tetraciclina. Na ausência desse antibiótico o mosquito macho morre. Por isso, as larvas do mosquito macho são criadas em laboratório na presença de tetraciclina. Quando o mosquito nasce ele é lançado na natureza para competir com os outros machos pelas fêmeas do Aedes. Espera-se que eles ganhem essa competição porque a prole que nascer morrerá, já que na natureza não há tetraciclina. O experimento é seguro porque os machos não picam seres humanos, só as fêmeas e são elas que transmitem a dengue. O experimento durará dois anos e a líder do projeto é uma pesquisadora brasileira da USP. Outro exemplo a demonstrar que estamos lentamente avançando é o novo pedido de pesquisadores da Embrapa para liberação planejada do feijão transgênico resistente ao vírus do mosaico dourado, desenvolvido inteiramente no Brasil.
Mas os produtos transgênicos que causam polêmica, por razões difíceis de compreender, são os alimentos. Os alimentos transgênicos são seguros e existem desde 1995. A exigência de regulamentações exageradas, com argumentos retóricos ao arrepio das evidências científicas, impõe o atraso aos países em desenvolvimento, notadamente nos países da África. Multinacionais poderosas não se importam com o dinheiro que têm de gastar para cumprir as exigências da estrita regulamentação. No entanto, pequenas empresas ou estatais como a Embrapa não têm orçamento suficiente para cumprir com tudo o que se lhes exige para a aprovação. O excesso de regulamentação favorece as empresas com muito poder econômico. Por isso, é imperioso iniciar a desregulação dessa área porque está provado que esses alimentos nada fazem ao ambiente e à saúde, ao contrário, são benéficos. Os interessados em informações científicas mais aprofundadas podem ler na íntegra os pareceres da CTNBio levados à votação para liberação comercial (http://www.ctnbio.gov.br/index.php/content/view/12786.html).
BIBLIOGRAFIA
ANDRADE, P. P.; NEPOMUCENO, A. L.; VIEIRA, M. L. C.; BARROSO, P. A. V.; TAPIAS, B. A.; COLLI, W. & PAIVA, E. Milho Geneticamente Modificado: Bases Científicas das Normas de Coexistência entre Cultivares. 1ª ed. Editora do Ministério de Ciência e Tecnologia, 2009. [ Links ]
BROOKES, G. & BARFOOT, P. "Global Impact of Biotech Crops: Socio-Economic and Environmental Effects in the First Ten Years of Commercial Use", in AgBioForum 9, 2006, pp. 139-51. [ Links ]
CÉLERES AMBIENTAL. The Social Environmental Benefits from Crop Biotechnology in Brazil: 1996-2009. Uberlândia, 2010 (www.celeresambiental.com.br). [ Links ]
DELANEY, B.; ASTWOOD, J. D.; CUNNY, H.; CONN, R. E.; HEROUET-GUICHENEY, C.; MACINTOSH, S.; MEYER, L. S.; PRIVALLE, L.; GAO, Y.; MATTSSON, J. & LEVINE, M. "Evaluation of Protein Safety in the Context of Agricultural Biotechnology", in Food Chem. Toxicol. 46, 2008, S71-S97. [ Links ]
FEDOROFF, N. & BROWN, N. M. Mendel in the Kitchen: A Scientist's View of Genetically Modified Foods. Joseph Henry Press, Washington, DC., 2004. [ Links ]
GOODMAN, R. E.; VIETHS, S.; SAMPSON, H. A.; HILL, D.; EBISAWA, M.; TAYLOR, S. & VAN REE, R. "Allergenicity Assessment of Genetically Modified Crops - What Makes Sense?", in Nature Biotech. 26, 2008, pp. 73-81. [ Links ]
JAMES, C. Global Status of Commercialized Biotech/GM Crops: 2009. ISAAA Brief nº 41, ISAAA, Ithaca, NY. [ Links ]
KEESE, P. "Risks from GMOs due to Horizontal Gene Transfer. Environ", in Biosafety Res. 7, 2008, pp. 123-49. [ Links ]
KEESE, P. Office of the Gene Technology Regulator. Risk Analysis Framework. http://www.ogtr.gov.au/internet/ogtr/publishing.nsf/Content/riskassessments-1. 2009. [ Links ]
MALARKEY, T. "Human Health Concerns with GM Crops", in Mutation Res. 544, 2003, pp. 217-21. [ Links ]
POTRYKUS, I. & AMMANN, K. "Transgenic Plants for Food Security in the Context of Development", in New Biotechnology 27, 2010, pp. 445-717. [ Links ]
RAYBOULD, A. "Problem Formulation and Hypothesis Testing for Environmental Risk Assessments of Genetically Modified Crops", in Environ. Biosafety Res. 5, 2006, pp. 119-26. [ Links ]
ROMEIS, J.; BARTSCH, D.; BIGLER, F.; CANDOLFI, M. P.; GIELKENS, M. M. C.; HARTLEY, S. E.; HELLMICH, R. L.; HUESING, J. E.; JEPSON, P. C.; LAYTON, R.; QUEMADA, H.; RAYBOULD, A.; ROSE, R. I.; SCHIEMANN, J.; SEARS, M. K.; SHELTON, A. M.; SEET, J.; VAITUZIS, Z. & WOLT, J. D. "Assessment of Risk of Insect-resistant Transgenic Crops to Nontarget Arthropods", in Nature Biotechnology 26, 2008, pp. 203-8. [ Links ]
VAN DEN BELT, H. "Debating the Precautionary Principle: 'Guilty until Proven Innocent' or 'Innocent until Proven Guilty'"?, in Plant Physiol. 132, 2003, pp. 1.122-6. [ Links ]
WATSON, J. D.; BERRY, Andrew. DNA: o Segredo da Vida. São Paulo, Companhia das Letras, 2007. [ Links ]
AGRADECIMENTOS
Agradeço a colaboração decisiva de Patrícia Fukuma aos comentários sobre a legislação pertinente, a William Barbosa pelos desenhos e a Alda Lerayer pelo fornecimento de dados socioeconômicos recentes e pela inspiração no desenho da Figura 3.